Nuestros servicios
REGULATORIO
Medicamentos de uso Humano y/o Veterinario
Descubre todo lo que podemos hacer en Konexio Biotech por tu negocio en todo aquello relacionado con los medicamentos de uso humano y/o veterinario.
- Apoyo regulatorio y generación de la estrategia a seguir (ROADMAPS)
- Revisión de la integridad y exactitud de los documentos regulatorios.
- Preparación y presentación de expedientes regulatorios a las entidades regulatorias.
- Realización de auditorías regulatorias sobre expedientes de registro.

Medicamentos
- Estrategia a seguir para obtener la aprobación más rápidamente (roadmaps), supervisión (auditorías del expediente) y gestión del proyecto.
- Asesorías científicas con la agencia reguladora.
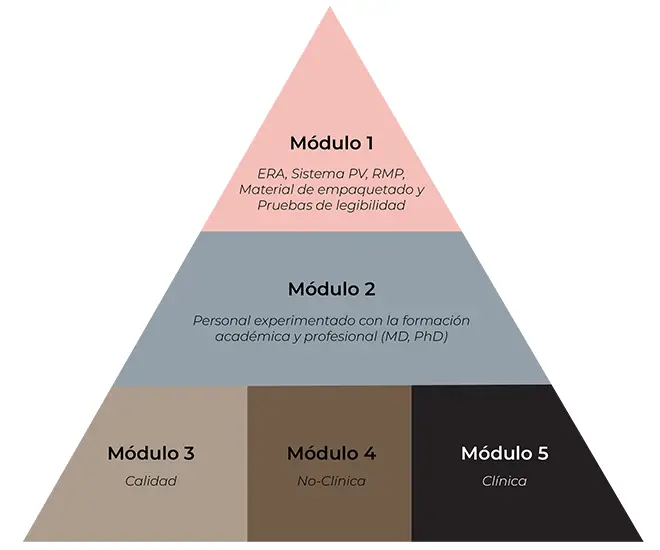
- Revisión, evaluación y desarrollo de todos los módulos:
Módulo 1: ERA, Sistema PV, RMP, Material de empaquetado y Pruebas de legibilidad
Módulo 2: Personal experimentado con la formación académica y profesional (MD, PhD)
Módulo 3: Calidad
Módulo 4: No clínica
Módulo 5: Clínica
Productos Sanitarios
- Generación de planes de gestión del riesgo de los productos.
- Obtención licencia de fabricante, importador, esterilizador o agrupador.
- Calificación y clasificación regulatoria de productos sanitarios.
- Preparación de expedientes técnicos para productos MDR e IVDR.
- Coordinación de Productos de fabricación “In House”
- Coordinación con los Organismos notificados.
- Obtención del marcado CE


Cosméticos
- Solicitud de Certificado de producto cosmético.
- Declaración responsable de actividades de fabricación y/o importación de cosméticos.
- Preparación del dossier de información y notificación.
- Preparación del informe de seguridad.
- Notificación al portal europeo.
Nutracéuticos
- Suplementos alimenticios.
- Registro de la empresa responsable del mercado en RGSEAA.
- Comunicaciones del primer producto puesto en el mercado.
- Modificaciones y cese de actividad.
- Registro de nuevos alimentos.
Nuestro proceso de trabajo
Descubre el proceso de trabajo que seguimos en Konexio Biotech para dar forma a tu proyecto de una forma integral.
Paso-01
Análisis regulatorio inicial
Evaluamos el marco regulatorio aplicable al producto, incluyendo la región objetivo y las clasificaciones necesarias para el cumplimiento normativo.
Paso-02
Desarrollo de la estrategia regulatoria
Diseñamos una hoja de ruta clara y personalizada para cumplir con los requisitos de las autoridades competentes, optimizando tiempos y recursos.
Paso-03
Elaboración de dossiers
Preparamos expedientes técnicos y regulatorios, incluyendo módulos de calidad, seguridad y eficacia, listos para su presentación ante las autoridades regulatorias.
Paso-04
Gestión de interacciones regulatorias
Actuamos como intermediarios con agencias como la EMA o FDA, gestionando consultas, solicitudes de aclaración y actualizaciones de los expedientes.
Paso-05
Soporte post-aprobación
Monitorizamos y gestionamos cambios regulatorios, renovaciones de licencias y actualizaciones necesarias para mantener la conformidad tras la aprobación del producto.
¿Quieres descubrir más sobre Regulatory Affairs?
Ofrecemos clasificación de dispositivos, elaboración de expedientes técnicos, preparación para auditorías y soporte en la obtención del marcado CE y otras aprobaciones globales.
Actuamos como enlace directo con agencias como la FDA, EMA y autoridades locales, facilitando reuniones, consultas científicas y presentaciones regulatorias.
Ayudamos en la preparación y presentación de Investigational New Drug (IND) y Clinical Trial Applications (CTA), asegurando el cumplimiento de los requisitos específicos de cada región.
Sí, contamos con experiencia en registros regulatorios en América, Latam, Europa, Asia y otros mercados emergentes.
Monitorizamos cambios normativos y ayudamos a mantener la conformidad mediante actualizaciones oportunas de los expedientes regulatorios y la documentación del producto.
Sí, aseguramos que los materiales de etiquetado cumplan con las normativas nacionales e internacionales y sean claros para los pacientes y profesionales de la salud.
Hemos trabajado con CAR-T, terapias génicas y medicamentos huérfanos, proporcionando estrategias regulatorias adaptadas a estas tecnologías innovadoras.
Evaluamos los requisitos específicos para productos combinados y preparamos estrategias regulatorias que abarquen tanto el componente farmacéutico como el dispositivo.
Sí, realizamos auditorías tanto internas como de proveedores para identificar áreas de mejora y garantizar el cumplimiento de las normativas regulatorias.
Sí, preparamos a las empresas para inspecciones y les asistimos durante y después del proceso para abordar cualquier hallazgo.

